
大腸直腸癌是世界上主要的腫瘤之一,死亡率在世界癌症死亡排名第三
根據台灣103年衛生署福利部統計處的統計數據
位居國人十大死因首位的惡性腫瘤中,大腸直腸癌的發生率排名第一
而男性或女性癌症死亡率排名都位居第三位 [1]
在美國2016年統計顯示,大腸直腸癌發生率排名第四名,死亡率則排名第二。 [1]
大腸直腸癌的形成,以腫瘤抑制基因突變或原致癌基因突變是大腸直腸癌形成的關鍵。
腫瘤抑制基因扮演著抑制正常細胞生長並促進細胞凋亡的角色。
一旦原致癌基因 (Proto-nocogene)突變形成致癌基因後,會造成其蛋白質產物過量產生或是活性增加,使細胞的生長及分裂大幅增加而導致癌症 [2]。
其中KRAS基因突變是促進大腸直腸形成的中邀基因之一
詳情請參考
1.RAS oncogene 簡介
2.RAS簡介-2 —尋找有效治療RAS mutation的方法
3.RAS簡介-3 —Cancer-specific hotspot
4.角色扮演遊戲—RAS參與的訊息傳遞路徑
5.期刊導讀:RAS如何走向細胞存活而引發癌症?
6.期刊導讀:維他命C可以選擇性地殺死KRAS及BRAF突變的大腸直腸癌細胞?
先前文獻證實,經常觀察到K-ras突變在密碼子12 (condon12)的位置發生突變,
當患者有KRAS condon12 突變時,會使患者的生存率下降。
所以,在臨床檢測KRAS condon12是否有發生突變的情形變成很重要的指標。
另外!!
大腸直腸癌的發生率極高,而且有趨向年輕化的情形
為更能夠提早發先提早治療~~
相應篩檢的方式也隨產生!!
在本篇主要講到的是與糞便潛血反應 (FOBT)有關的技術。
糞便潛血反應 (FOBT)是什麼?
糞便潛血代表的就是糞便中存在微量的血液,一般肉眼難以觀察出來,所以需要透過儀器進一步檢測。如果檢測出陽性反應,表示消化道中某個部分可能出現問題而造成消化道出血,原理是當消化道出血時,血液會附著在糞便表面,一同被排出去。這個是大腸直腸癌最常使用的篩檢工具之一 [3]。
FOBT的優勢是不具侵入性,且能夠方便快速檢測出結果,但是準確性卻比較低(有偽陽性的可能),還是需要透過大腸鏡來進一步確認。或另外加做基因檢測來看與大腸直腸癌相關度比較高的基因來輔助確診 [3]。
而在這項研究中,則開發了一種從人類糞便中提取結腸細胞RNA的方法。
以此檢測人類糞便中的基因,促進大腸直腸癌的早期檢測和預防。
實驗結果中~~
在糞便中的檢測率比結腸癌組織和體細胞的DNA還高 (圖A)。
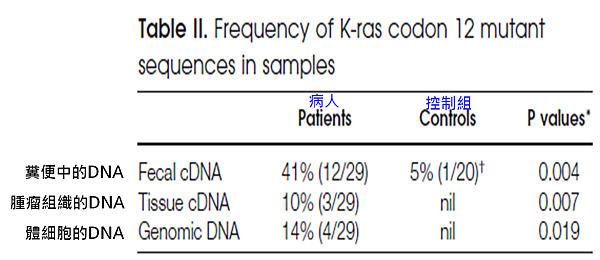
圖A. 不同檢體檢測KRAS的結果
這些數據表明,在糞便K-ras突變可能比在單個癌組織塊中更多樣化。
代表從CRC患者的糞便中分離的K-ras突變體的多樣性可能來自不同腫瘤的組織。
也可能是結腸壁各部分的細胞狀態不佳,所導致的結果。
也可證實從CRC患者和健康對照的整個結腸的上皮細胞比較,已證實大腸癌患者的糞便具有K-ras突變的情形。
這些結果也證實了K-ras密碼子12突變與年齡呈正相關 (圖B)。
平均年齡59歲以上的患者K-ras密碼子12突變的概率增加
這也說明CRC的風險隨著年齡的增長而升高
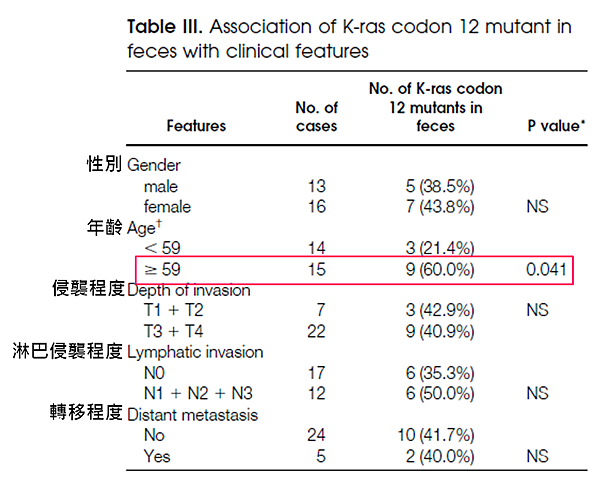
圖B. KRAS基因突變與年齡的關係
![]() 總之
總之![]()
![]() 糞便檢體萃取出的結腸細胞的RNA分析用於輔助診斷CRC。
糞便檢體萃取出的結腸細胞的RNA分析用於輔助診斷CRC。
![]() 這大腸癌患者的糞便中,可檢測出KRAS基因突變
這大腸癌患者的糞便中,可檢測出KRAS基因突變
![]() 大腸癌患者糞便中常見的是KRAS condon12的基因突變
大腸癌患者糞便中常見的是KRAS condon12的基因突變
![]() 大腸癌的發生率的確會隨著年齡增加而風險增加
大腸癌的發生率的確會隨著年齡增加而風險增加
![]() 此技術可適用於篩选和確定K-ras基因在糞便中的臨床意義,使患者可以受益。
此技術可適用於篩选和確定K-ras基因在糞便中的臨床意義,使患者可以受益。
參考資料:
- 大腸直腸癌簡介
- 大腸直腸癌形成 — 什麼基因在作怪?
- 糞便潛血反應(FOBT)的臨床瓶頸與解決方案
- Rozen P. Cancer of the gastrointestinal tract: early detection or early prevention? Eur J Cancer Prev 2004;13:71–5.
- Correlation of K-ras codon 12 mutations in human feces and ages of patients with colorectal cancer (CRC)
- Davies RJ, Miller R, Coleman N. Colorectal cancer screening: prospects for molecular stool analysis. Nat Rev Cancer 2005;5:199–209.
- Haug U, Brenner H. A simulation model for colorectal cancer screening: potential of stool tests with various performance characteristics compared with screening colonoscopy. Cancer Epidemiol Biomarkers Prev 2005;14:422– 8.
- Bandaletova T, Bailey N, Bingham SA, Loktionov A. Isolation of exfoliated colonocytes from human stool as a new technique for colonic cytology. APMIS 2002;110:239–46.
- Iyengar V, Albaugh GP, Lohani A, Nair PP. Human stools as a source of viable colonic epithelial cells. FASEB J 1991;5:2856 –9.


 留言列表
留言列表

