老化可以定義為正常身體功能的逐漸產生生物性的損傷,並伴隨著對壓力反應的能力降低和顯著的增加發病率和死亡率的風險,這種複雜和多因素參與的老化過程對器官的功能及整個生物體的功能產生直接影響,最終導致健康狀態惡化,其中最具代表性的疾病包括癌症,心血管疾及神經退化性疾病。由於這過程涉及多種的機制,目前希望能更深入地了解老化的分子機制,並期望能應用於延長人類壽命為深遠的目標。
最近已有科學家精確地定義所謂的“老化表型 (Aging phenotype)”將這些標誌分為三個不同的類別:
- 主要標誌 (Primary hallmarks):為最初觸發衰老過程,例如DNA損傷,端粒丟失 (Telomere loss)和表觀遺傳 (Epigenetic alterations)改變。
- 拮抗標誌 (Antagonistic hallmarks):最初保護生物體免受損害,但在主要促進的整個過程中會促進細胞受損,例如反應性氧化物 (Reactive Oxygen Species, ROS)。
- 整合性標誌 (Integrative hallmarks):當導致損傷累積的過程變得不可逆時,直接損害體內平衡,例如炎症或乾細胞衰竭。
基因組不穩定性 (Genomic instability)被認為是衰老過程的主要驅動因素。實際上,在細胞壽命期間,基因組DNA持續暴露於不同危害破壞其完整性和功能性, 而DNA可能受到外源性環境因素或內源性化學物質的攻擊,可分為:
- 外源性環境因素 (Exogenous environmental factors):氧化壓力,遺傳毒性藥物和電離輻射。
- 內源性化學物質 (Endogenous chemicals):正常線粒體代謝的副產物ROS、DNA複製錯誤和自發水解反應。
如果DNA損傷沒有被適當修復,則它們將被轉化為永久突變,導致增加罹患癌症的風險,此外,DNA損傷也可以引起DNA合成及複製停止,導致細胞衰老或細胞死亡,從而開始促進細胞衰老的過程,因此,癌症和老化,都是由於不可挽回的DNA損傷的結果,就像是同一枚硬幣的兩面,一體兩面的概念,在老化過程中,DNA損傷率的增加是源自細胞代謝的副產物的產生和處置之間的不平衡的總體結果,以及DNA修復效率的功能下降。

圖A. 促進老化的機制簡圖
為了應對細胞內的DNA損傷,細胞已發展出針對不同DNA損傷所產生的修復機制,稱作DNA損傷反應 (DNA Damage Response, DDR),是一種複雜且可精細調節的基因組的修復系統,可以感測並發出傳遞訊號告知DNA損傷的存在,最終促進其進行DNA修復。
DDR機制可以分成下列幾種:
- 單股DNA修復 (Single Strand Breaks, SSBs)
- 直接修復機制 (Direct reversal)
- 鹼基切除修復 (Base Excision Repair, BER)
- 核苷酸切除修復 (Nucleotide Excision Repair, NER)
- 錯誤配對修復(Mismatch repair, MMR)
- 單股DNA斷裂修復(Single strand break repair, SSBR)
- 雙股DNA修復 (Double Strand Breaks, DSBs)
- 同源性重組 (Homologous Recombination, HR)
- 非同源性末端接合 (Non-Homologous End Joining, NHEJ)
DDR機制可以影響許多細胞生長重要的過程,例如DNA復制 (DNA replication)、轉錄 (Transcription)、細胞週期進程 (Cell cycle progression)、染色質重塑 (Chromatin remodeling)、分化 (Differentiation)、凋亡 (Apoptosis)、信號傳導和反應系統。此外,DDR機制可以觸發不同的DNA修復途徑,每個DNA修復途徑針對特定類別的DNA損傷,目的在於恢復DNA化學結構的完整性。
那p53家族在DNA受損、細胞凋亡及老化的過程中具有甚麼功能?
p53家族的成員有p53、p63及p73,每個成員可以作用於獨特的靶標,因此,這些蛋白質在細胞中可以發揮不盡然完全重疊的作用。p53家族蛋白質能參與不同DDR的誘導,以活化或啟動相關的機制來決定細胞的命運。此外,他們亦可以促進短暫的細胞週期停滯來進行適當的DNA修復以防止潛在的腫瘤細胞分裂,在連續或不可修復的DNA損傷的情況下,則會永久的停滯細胞週期的運行,導致細胞衰老,細胞的型態會變成擴大和扁平化的形狀,且基因表達和染色質結構會有顯著的變化。p53及其家族成員最常探討的功能是細胞凋亡的調控,而p53蛋白的促凋亡功能依賴於其他轉錄因子的調控,例如c-Myc。
老化的機制目前已知是由兩個獨立的途徑驅動細胞老化的過程,各別為p53-p21路徑及p16-Rb路徑。p21和p16都是細胞週期蛋白依賴性激酶抑製劑 (Cyclin-dependent kinase inhibitors, CDKI),可以防止Rb被磷酸化,來抑制Rb活化,總體的作用是抑制E2F轉錄因子的活性,來抑制細胞週期的運行。p53、p63及p73都可以直接誘導p21蛋白的活化,使細胞週期停滯。p53、p63和p73可以一起合作來調節細胞生存、死亡和衰老之間的平衡。總之,p53家族成員可以促進和抗衰老作用取決於其他調節因子的存在,更多地是取決於細胞環境。
儘管p53家族對於老化機制的調節不太明顯,p53家族成員仍可以透過相關功能,例如DNA修復機制的功能來減緩細胞衰老的作用。p53可以透過與染色質重塑相關之蛋白作用調控其DNA修復,以維持細胞存活及減緩老化;p53-p21路徑可以維護基因組的穩定性以防止衰老的過程,也可作為生物反應的調節劑可根據損傷的程度引導細胞進行DNA修復或朝向衰老。p63類似於p53,p63能促進致癌所誘導的衰老,若缺乏p63則會加速衰老。p73可通過維持標的穩定狀態來防止衰老的自噬。
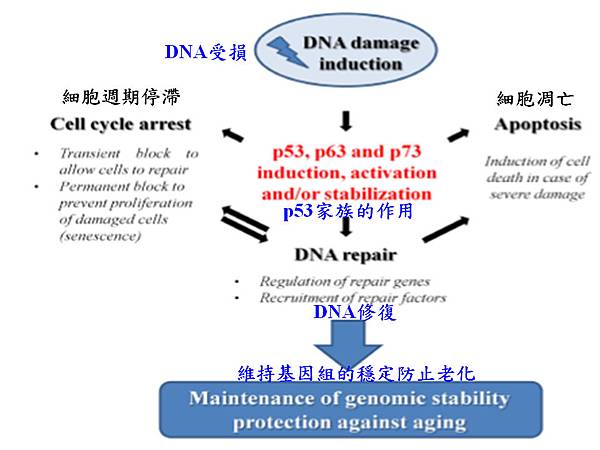
圖B. 防止老化的機制簡圖
基因組不穩定性與衰老過程密切相關。由於DNA的完整性受到內源和外源因素的持續攻擊,保護基因組完整的機制可以作為抗衰老的標的機制。鑑於這些科學性證據,p53家族在維持基因組穩定性發揮關鍵的作用,因此,他們的功能能夠影響複雜的老化過程。
參考資料:
Sara Nicolai, et al. 2015. DNA repair and aging: the impact of the p53 family. AGING. Vol. 7 No.12.


 留言列表
留言列表

