身體老化的現象引起普羅大眾熱衷於抗老化的活動或醫療行為,例如;醫療美容、再生醫學 (Regenerative medicine)或回春療法 (Rejuvenation medicine)。過去文獻中,科學家利用基因工程的方式使老鼠的粒線體聚合酶 (Mitochondrial polymerase)的校正效率變差,使粒線體DNA在進行合成時容易發生錯誤,實驗結果證實粒線體DNA突變的確會加速老鼠的老化。此外,在端粒酶缺陷的老鼠體內會造成粒線體功能異常,使體內組織萎縮、幹細胞耗盡、器官衰竭及組織無法進行修復的情形產生,最終導致老化,而且有許多研究也發現在百歲人瑞體內的端粒酶的長度與人類壽命有正向關聯性,也就是端粒酶較長的人,整體的健體概況有顯著的改善,且與年齡相關之疾病的發病率普遍較低、認知功能和脂質代謝的狀況較一般長度端粒酶的人有得到明顯的改善。目前已證實粒線體DNA (Mitochondrial DNA, mtDNA)發生突變是主要能夠驅動體內多種系統老化的主要原因之一,在人類老化的過程中,粒線體DNA會由於體內不斷產生氧化壓力所導致的DNA受損或是在DNA進行複製和合成所形成的錯誤配對等原因,導致這些基因序列錯誤,簡單說也就是突變,持續性的在體內的細胞中累積,造成細胞進行性的邁向老化的深淵。
現代慢性疾病主要源於久坐的生活方式和過量的能量攝入,科學家已提出無可置疑的證據表明,運動的確能增加端粒酶活性和減少衰老標誌物 (Senescence markers)的產生 [2],其中,耐力運動 (Endurance exercise)延長了預期壽命,降低了囓齒動物和人類的慢性疾病的風險 [3,4],但其詳細的機制仍是未知的。
研究者利用基因工程的方式建立一個早衰的老鼠動物模式,也就是讓粒線體聚合酶-γ (Mitochondrial polymerase gamma, POLG1-γ)發生突變,而無法在DNA合成並複製完成時進行校對,造成基因序列錯誤而導致突變,接著對動物實施耐力運動的計畫來檢測老鼠體內老化相關分子的表現及老鼠的行為表現,來探討延緩老化的機制。研究結果發現耐力運動可以使p53蛋白進入到粒腺體內活化非POLG1-γ的DNA修復機制並調控粒腺體內的合成代謝系統,進一步能夠降低粒線體發生突變的機率並延長動物的存活時間。這篇文章發現p53可以透過運動的刺激而促進基因修復,此外,p53也可作為粒線體基因突變相關的疾病的新型治療模式。
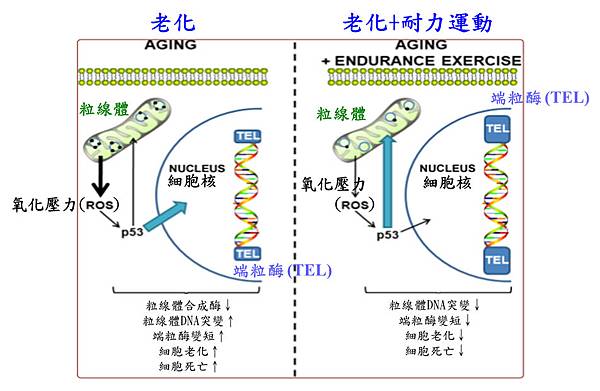
圖A. 老化及耐力運動的關聯圖
參考文獻:
1. Adeel Safdar, et al. 2016. Exercise-induced mitochondrial p53 repairs mtDNA mutations in mutator mice. Skeletal Muscle. 6:7.
2. Wolf SA, Melnik A, Kempermann G. 2011. Physical exercise increases adult neurogenesis and telomerase activity, and improves behavioral deficits in a mouse model of schizophrenia. Brain Behav Immun.
3. Stessman J, Hammerman-Rozenberg R, Cohen A, Ein-Mor E, Jacobs JM. 2009. Physical activity, function, and longevity among the very old. Arch Intern Med. 169(16):1476–83.
4. Chakravarty EF, Hubert HB, Lingala VB, Fries JF. 2008. Reduced disability and mortality among aging runners: a 21-year longitudinal study. Arch Intern Med. 168(15):1638–46.


 留言列表
留言列表

