
Different EGFR Gene Mutations in Exon 18, 19 and 21 as Prognostic and Predictive Markers in NSCLC: A Single Institution Analysis
Mol Diagn Ther. 2016 Feb; 20(1):55-63. doi: 10.1007/s40291-015-0176-x.
不管在男性或女性,肺癌為癌症導致死亡的主因之一,
而其中有75-80%的患者具有
非小細胞肺癌(NSCLC)組織病理的特性[1]。
早期對於轉移的NSCLC是以金屬鉑為基礎的化學療法,而隨著致癌分子機制的發現,在近期則慢慢轉為以表皮生長因子受體(EGFR)為治療的模式,EGFR為細胞膜上ETBB酪氨酸受體的家族成員之一,主要會調控血管新生、細胞增生、細胞凋亡以及活化上皮細胞間質轉化[2,3],然而當NSCLC患者的EGFR基因產生突變時,對EGFR抑制劑(TKIs:gefitinib, erlotinib, afatinib)有較好的反應,同時也增加患者的OS總生存(約20週)[4,5]。
在許多回顧性及前瞻性的研究中都證實具有EGFR突變之患者對TKIs的反應率約為70-80%,另外一些NSCLC臨床因素,如:從未吸菸、女性、亞洲人、肺腺癌病史也都與EGFR基因突變有關[6]。EGFR突變常見於酪氨酸激酶基因前四個exon當中,而其中有90%為exon 19的缺失或是exon 21的點突變(p.L858R)[7],另外exon 18及exon 20的突變較為少見,各占所有EGFR突變的4%左右[8]。
部分臨床數據統計,具有exon 19缺失的患者比exon 21點突變的患者有較長OS總生存[9,10],然而在這些突變與患者使用TKIs後的預後及臨床反應還並不清楚,因此本實驗的目的為分析exon 18、19及21在接受TKIs治療之患者預後的結果。
本實驗分析55位具有已轉移之NSCLC患者(表一),並利用石蠟包埋檢體偵測其EGFR突變情形(exon 18,19和21的突變),並統計2004到2014年的數據資料,分析其總生存OS (Overall survival)及疾病進展時間TTP (Time to progression)。
[註]
OS:從隨機化開始至(因任何原因)死亡的時間;
TTP:從隨機化開始到腫瘤發生(任何方面)進展或(進展前)死亡之間的時間)[11]。

表一、受測者資料統計
結果顯示,有43人死亡(78%),其中exon 18突變組有5人(100%),exon 19突變組有23人(72%),在exon 21突變組則有15人(83%)。腦/腦膜轉移被公認為預後重要的指標之一,在其中exon 18突變組有1人(20%),exon 19突變組有16人(50%),在exon 21突變組則有6人(33%)。在exon 19突變組有最長的中位數OS (22.73個月),相較於exon 18突變組 (11.26個月)及exon 21突變組(16.16個月)高出許多(圖一)。

圖一、Exon 18、19及21各組之總生存OS
而經過TKIs治療的患者,在exon 19突變組與exon 21突變組在TTP並沒有顯著的差異(13.4 vs. 11.3 months; p = 0.89),相反地exon 18突變組為最差的(圖二)。
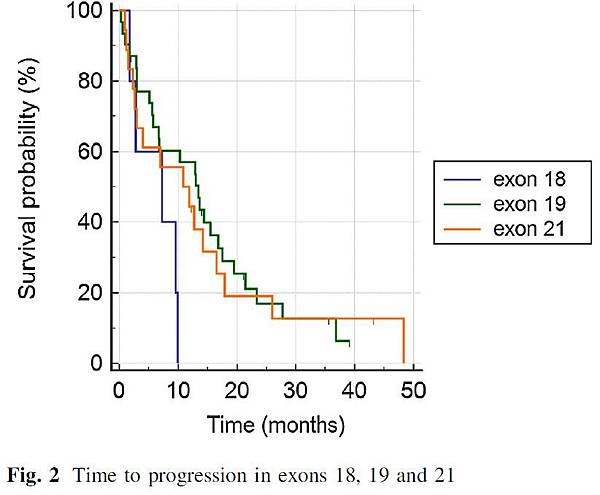
圖二、Exon 18、19及21各組之疾病進展時間TTP
統計患者對TKIs的反應率,在exon 18、19及21突變組各別為40%、71.8%及66.6%,顯示exon 18突變組反映最差(表二)。

表二、Exon 18、19及21各組對TKIs的反應率
結論:
(1)exon 19突變儘管有較高的腦轉移率,但是卻有較佳的OS及TTP
(2)然而exon 18突變雖然發生率低,但是其OS及TTP都不好,同時對TKIs的反應率也不佳。
因此可知,當診斷出NSCLC時,鑑別是否具有EGFR突變對於療程是一個很重要的參考數值,同時也會影響患者腫瘤轉移及預後結果。
Edited by A-Kai
參考資料:
1. 1. Ferlay J, Soerjomataram I, Dikshit R, Eser S, Mathers C, Rebelo M, Parkin DM, Forman D, Bray F. Int J Cancer. 2015;136(5):E359–86.
2. Larsen AK, Ouaret D, El Ouadrani K, Petitprez A. Pharmacol Ther. 2011;131:80–90.
3. Barr S, Thomson S, Buck E, et al. Clin Exp Metastasis. 2008;25:685–93.
4. Paz-Ares L, Soulie`res D, Melezı´nek I, Moecks J, Keil L, Mok T, Rosell R, Klughammer B. J Cell Mol Med. 2010;14(1–2):51–69.
5. Pao W, Miller V, Zakowski M, et al. Proc Natl Acad Sci USA. 2004;101:13306–11.
6. Miller VA, Kris MG, Shah N, Patel J, Azzoli C, Gomez J, Krug LM, Pao W, Rizvi N, Pizzo B, Tyson L, Venkatraman E, Ben- Porat L, Memoli N, Zakowski M, Rusch V, Heelan RT. J Clin Oncol. 2004;22(6):1103–9.
7. Kosaka T, Yatabe Y, Endoh H, Kuwano H, Takahashi T, Mitsudomi T. Cancer Res. 2004;64(24):8919–23.
8. Beau-Faller M, Prim N, Ruppert AM, Nanni-Mete´llus I, Lacave R, Lacroix L, Escande F, Lizard S, Pretet JL, Rouquette I, de Cre´moux P, Solassol J, de Fraipont F, Bie`che I, Cayre A, Favre-Guillevin E, Tomasini P, Wislez M, Besse B, Legrain M, Voegeli AC, Baudrin L, Morin F, Zalcman G, Quoix E, Blons H, Cadranel J. Ann Oncol. 2014;25(1):126–31.
9. Morita S, Okamoto I, Kobayashi K, Yamazaki K, Asahina H, Inoue A, Hagiwara K, Sunaga N, Yanagitani N, Hida T, Yoshida K, Hirashima T, Yasumoto K, Sugio K, Mitsudomi T, Fukuoka M, Nukiwa T. 2009;15(13):4493–8.
10. Riely GJ, Pao W, Pham DK, et al. Clin Cancer Res. 2006;12:839–44.
11. https://read01.com/n4EQPM.html


 留言列表
留言列表

